سینتک شیمیایی
جهان امروز از نداشتن دارویی به نام پرهیز و اخلاق رنج می برد. (ماری کوری)سینتک شیمیایی
جهان امروز از نداشتن دارویی به نام پرهیز و اخلاق رنج می برد. (ماری کوری)عوامل موثر بر سرعت واکنش های شیمیایی
نوع مواد شرکت کننده در واکنش یا ماهیت مواد شرکت کننده در واکنش :
توجه داریم که سرعت واکنش سدیم با آب به مراتب از واکنش آهن با آب بیشتر است . چنین تفاوتی در سرعت واکنش ها را به تفاوت در ماهیت یا خواص این مواد نسبت می دهیم .
حالت فیزیکی :
می دانیم که حالت فیزیکی یک ماده به دما بستگی دارد و برای یک ماده معین با افزایش دما تغییر حالت از جامد به مایع و سرانجام به گاز صورت می گیرد لذا بدیهی است که سرعت واکنش در حالت گازی نسبت به حالت های متراکم ماده بیشتر باشد .
اما در دمای ثابت می توان با انحلال مواد در حلال مناسب امکان برخورد مناسب تر ذرات با یکدیگر را فراهم نمود و سرعت واکنش را افزایش داد .
غلظت :
معمولا افزایش غلظت موجب افزایش سرعت واکنش های شیمیایی می شود زیرا افزایش غلظت باعث افزایش تعداد برخورد ها می گردد . در بسیاری از واکنش ها دو برابر شدن غلظت هر یک از واکنش دهنده ها با دوبرابر شدن سرعت واکنش همراه است ولی این موضوع کلی نمی باشد . زیرا افزایش تعداد برخورد همواره موجب افزایش سرعت نمی شود . دلیل این امر آنست که لازمه انجام واکنش داشتن یک حداقل انرژی (همان انرژی فعالسازی ) ذرات واکنش دهنده است . که با افزایش تعداد ذرات متفاوت است .
برای درک بهتر چگونگی وابستگی سرعت واکنش با غلظت واکنش دهنده ها ضروری است به رابطه ی قانون سرعت برای واکنش مورد نظر واقف باشیم . این رابطه نیز به نوبه ی خود از طریق تجربه و آزمایش قابل حصول است .
واکنش فرضی :
aA + bB → cC را در نظر می گیریم رابطه قانون سرعت برای این واکنش به صورت زیر نوشته می شود :
در این رابطه:
k ثابت سرعت بوده وکمیتی تجربی است، n و m رابه ترتیب مرتبه سرعت نسبت به هر یک از گونه های A و B گویند . لازم به ذکر است که n و m ارتباطی به ضرایب استوکیومتری نداشته و از طریق تجربه و آزمایش تعیین می شوند .
افزایش فشار یک گاز یا افزایش مساحت سطح یک واکنش دهنده ناهمگن موجب افزایش سرعت واکنش می گردد .
چرا افزایش فشار اثر مشابه افزایش غلظت بر سرعت یک واکنش گازی دارد ؟
رابطه ی قانون سرعت ٬ چگونگی وابستگی سرعت واکنش به غلظت واکنش دهنده ها و مرتبه ی واکنش;
مثال :
رابطه ی قانون سرعت را برای واکنش داده شده نوشته و سپس :
HgCl2(aq)+C2O42--> 2Cl-(aq)+2CO2(g)+Hg2Cl2(s)
1) مرتبه واکنش را نسبت به هر جز تعیین نمایید ؟
2) مرتبه کلی واکنش را تعیین نمایید ؟
3) اگر غلظت همه ی واکنش دهنده ها بطور همزمان دو برابر شود سرعت واکنش چند برابر خواهد شد ؟
آزمایش | [C2O42-] | [HgCl2] | سرعت اولیه واکنش (مول بر لیتر بر دقیقه) |
1 | .125M | .204M | 2.4x10-5 |
2 | .25M | .204M | 9.6x10-5 |
3 | .25M | .102 | 4.7x10-5 |
چگونگی اثر دما و کاتالیزگر بر سرعت واکنش های شیمیایی : (رابطه آرنیوس)
افزایش دما معمولا به افزایش سرعت واکنش می انجامد زیرا تعداد برخوردها زیاد می شود و بیشتر برخورد ها از انرژی کافی برای تشکیل پیچیده ی فعال (کمپلکس فعال ) برخوردارند .
برای بررسی اثر دما و کاتالیزگر بهتر است با رابطه ی آرنیوس که چگونگی وابستگی ثابت سرعت با دما و انرژی فعالسازی را نشان می دهد آشنا شویم :
Ea/RT -
k = A e
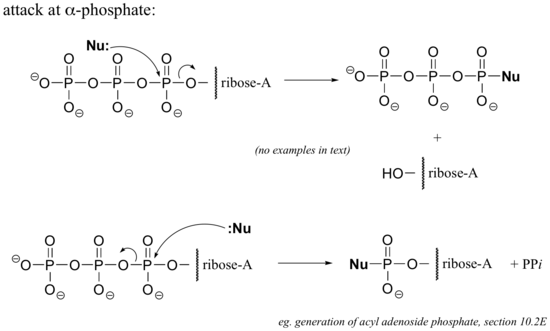
دما و کاتالیزگر با تغییر ثابت سرعت ؛ سرعت واکنش را تغییر میدهد :
1) همچنانکه در منحنی مشاهده می شود افزایش دما باعث افزایش مقدار عددی ثابت سرعت می شود .
2) استفاده از کاتالیزگر باعث می شود انرژی فعالسازی واکنش کاهش یافته و ثابت سرعت افزایش یابد .
اگر چه ممکن است تغییر انرژی در بسیاری از واکنش های شیمیایی منفی باشد ، ولی اغلب این واکنش ها به مقداری انرژی ورودی اولیه نیاز دارند تا بتوانند پیچیده ی فعال تشکیل دهند این انرژی مورد نیاز را انرژی فعالسازی گویند . به بیان دیگر :
انرژی فعالسازی حداقل انرژی لازم برای شروع واکنش است .
کاتالیزگر دما
کاتالیزور ماده ای است که سرعت واکنش را زیاد می کند و خود دچار تغییر دائم نمی شود .